Schématický
zápis
|
| Nitrobenzen
působí -M efektem, tudíž má nižší
celkovou elektronovou hustotu, ale v polohách 3 a 5
vyšší. Elektrofilní činidlo jde do polohy 3. |
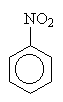 |
+ HNO3 |
|
 |
|
Podrobný
zápis
|
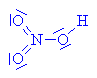
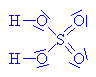
| Kyselina
sírová daruje vodíkový kation
(Lewisova kyselina)
kyselině dusičné
(Lewisova kyselina)-
váže se na volný elektronový pár u kyslíku |
|
|
|
|
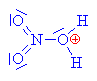
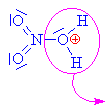
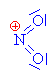
| Kation odštěpuje vodu a vzniká
tak nitroniový kation, který je elektrofilním
činidlem |
|
|
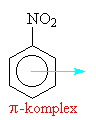
| Nitroniový kation se napojuje na aromatický systém
benzenu přes tzv. p komlex.Nitrobenzen působí
-M
efektem, tudíž má nižší celkovou elektronovou
hustotu, ale v polohách 3 a 5 vyšší. Elektrofilní
činidlo jde do polohy 3. Zjednodušeně a názorněji (i
když poněkud nepřesně) se dá říci, že v poloze 3
se na dvojnou vazbu (konjugovaného 6 -ti elektronového
systému) napojuje elektrofilní činidlo |
|
|
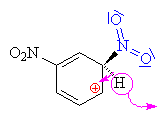
| Aromatické jádro přestalo existovat, na sousedním
uhlíku od napadeného je kladný náboj (má pouze 3
vazby - 2 s uhlíky a jednu s vodíkem)- vznikl tzv. s komlex , je velká snaha obnovit
stabilní aromatické jádro: |
|
|
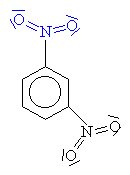
| Při obnování stabilního aromatického jádra se
odpojuje vodíkový kation a jím uvolněná vazba se
zapojuje do jádra a tak opětně vzniká stabilní
aromatický 6 elektronový kruh. Vznikl 1,3-dinitrobenzen |
|
|
| Odštěpený vodíkový kation se napojuje na hydrogensulfátový
anion a za vzniku kyseliny sírové
(ta tedy slouží jako katalyzátor) a ta rozbíhá další kolo reakce |
|
|