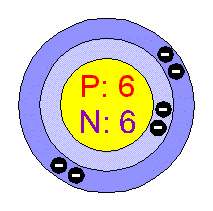

-je to velice důležitý biogenní prvek, čistý uhlík se vyskytuje buď v modifikaci diamantu nebo tuhy, které mají naprosto rozdílné vlastnosti. Diamant krystalizuje v krychlové soustavě a to nejčastěji v osmistěnech, jsou buď bezbarvé a průhledné anebo různě zabarvené, ale všechny velice dobře lámou světlo. Diamanty jsou n
ejtvrdší přírodní látkou na Zemi, proto se některé jeho neprůsvitné formy používají k řezání skla, kovů a kamenů. Dá se také při vyšší teplotě zapálit a shoří na oxid uhličitý. Naproti tomu u tuhy (grafitu) krystalizuje uhlík v šestiúhelníkových šupinkách, které se lehko odštěpují podél vrstev. Krystaly tuhy jsou velice měkké a špiní, i přesto má tuha rozsáhlé použití např. výroba elektrod, tužek, různých žáruvzdorných předmětů, mazadel, moderátorů pro jaderné reaktory (zpomalení neutronů ) apod. Modifikace diamantu je nestálá, a proto se samovolně přeměňují na tuhu. Avšak většinou ho nacházíme ve formě obyčejného uhlí rozličných kvalit od lignitu až po černé uhlí a nejkvalitnější antracit. Uhlí vzniklo zuhelnatěním pravěkých rostlin v bahně bez přístupu vzduchu (karbon).Vznikali i jiné vodíkaté sloučeniny s uhlíkem (ropa a zemní plyn).Člověk vymyslel svou vlastní formu a to dřevo pálené za nepřístupu vzduchu - tzv. dřevěné uhlí, které na svém velkém povrchu zachycuje zápachy tuků a jedovatých látek. Karbonizací (suchou destilací ) čili zahříváním uhlí za nepřístupu vzduchu vzniklé tzv. koks, který je potřebný na redukci kovů z rud. Druhým produktem při tomto procese je svítiplyn, který se dříve používal na místo zemního plynu. Živočišné uhlí využívané při střevních potížích se získává spalováním krve. Uhlík reaguje s kovy za vzniku karbidů např. vápenatý, z kterého se působením vody vyrábí acetylén. Smrtelně jedovatý je oxid uhelnatý vzniklý nedokonalým spalováním.-po kyslíku je to nejvíce zastoupený prvek v zemské kůře.Z magmatu krystalizuje křemen přes několik modifikací.Z křemene se vyrábí sklo, které bylo známo již ve starém Egyptě. Některé odrůdy křemene jsou známé drahokamy mimo průzračného křišťálu, který se používá na výrobu hranolů na optické přístroje, to jsou žlutý citrín,hnědá záhněda růžový růženín, fialový ametyst, červený karneol nebo černý morion a mnoho dalších.Z amorfních odrůd je to např. pazourek, polodrahokamové odrůdy jako jsou opály, acháty, chalcedóny atd. Používá se jednak v keramickém průmyslu, ale také je základem žáruvzdorného materiálu, který je se používá v různých průmyslových odvětvích.
-tento kov je rozptýlen a často doprovází křemičitany,zinkové a také cínové rudy.Je to křehký šedobílý kov, který je svými vlastnostmi podobný cínu nebo křemíku, je typickým polovodičem s nízkou elektrickou vodivostí, která závisí na teplotě.Je také velice drahý.Germanium se používá také v radiotechnice, avšak na tyto účely je třeba plně vyčištěné, to znamená, že na 1miliard
u atomů je přípustný pouze 1atom nečistoty.Avšak použití germania v praxi je zatím ve stádiu vývoje.-jeho nejznámější rudou je cínovec neboli kasiterit SnO
2.Cín se vyrábí redukcí cínovce koksem v šachtové peci, je to krystalický stříbrolesklý, měkký, velice kujný kov.Slouží jako ochranný povrch na železné plechy, z kterých se vyrábějí konzervy, protože cín odolává kyselým šťávám a potraviny se v něm nekazí.Slitina s antimonem a mědí se nazývá "královský cín", ze kterého se vyrábí příbory a konvice atd.Je to velice deficitní kov, kterým je třeba šetřit, proto např. klempířská pájka může obsahovat jen 15% cínu na místo původních 30 - 60%.Zajímavý jev uvidíme, když cínové předměty vystavíme mrazu, objeví se nich šedé body, které se zvětšují až se úplně spojí,a to proto že jde o přeměnu bílého cínu na práškovou modifikaci šedého cínu. Tento rozpad je úplný při -33 stupních a je možné ho přenést z kovu na kov jako chorobu "cínový mor",jeho zastavení je možné pouze zvýšením teploty na +20 stupňů.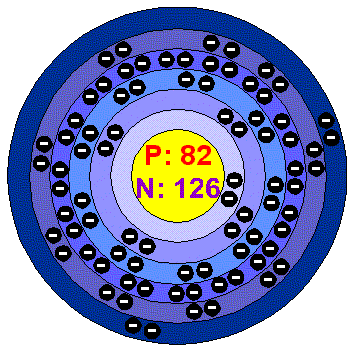
-nejznámější rudou je galenit PbS.Olovo se vyrábí pražením galenitu na oxid a síran olovnatý, ze kterých se další reakcí s galenitem dostává surové olovo,což se rafinuje elektrolyticky. Je to měkký modrobílý kov, 50-krát měkčí než ocel. Je ho dokonce možné krájet nožem a psát s ním na papír.Na vzduchu se pasivuje, je ho možné velice dobře tvarovat. Z olověného plechu se dokonce zhotovují odpařovací pánve na výrobu kyseliny sírové.Z olova se též vyrábějí ochranné kryty, ochranné stěny proti radioaktivnímu a rentgenovému záření, akumulátory trubky na vodovody, které se v současnosti již více nahrazují trubkami z umělé hmoty.Kyselina uhličitá rozpuštěná ve vodě pokrývá stěny bílou vrstvičkou zásaditého uhličitanu olovnatého,což zabraňuje dalšímu rozpouštění olova a tím i otravám.Z toho vyplývá, že olovo i všechny jeho sloučeniny jsou jedovaté.Pb se používá jako hlavní příměs do řady slitin. Olovo vzniká v přírodě jako konečný produkt rozpadu radioaktivního radonu.Zajímavé je, že staré obrazy, které jsou malované olovnatou bělobou- zásaditým uhličitanem olovnatý postupem času černají a to v důsledku sirovodíku ve vzduchu, ale je možné získat původní barvu nazpátek peroxidem vodíku.