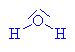
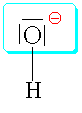
| Lze
odhadnout pH alkoholů a fenolů v porovnání s vodou???Odpověď zní - ano zásluhou
působících efektů. Pamatuj tuto
zásadu: sloučenina se "snaží"
mít co nejmenší náboj. Pokud má vzniknout ion (ať
už kation nebo anion) "ochotněji" vznikne
tam, kde je náboj kompenzován částečným nábojem
opačného znaménka, neboli tam, kde je náboj v
absolutní hodnotě menší než jedna. Nejhůře pak
tam, kde naopak je náboj větší v absolutní hodnotě
než jedna. |
| Je známo, že kyselina odštěpuje
vodíkové kationty a důsledku toho má pH menší než 7. Zásada naopak
vodíkové kationty přijímá a v důsledku toho má pH větší než 7. |
 |
 |
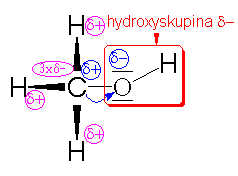
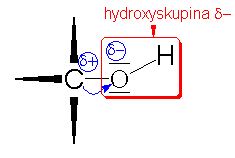
U alkoholu
působí +I efekt, který způsobuje
alkylová skupina na uhlíku sousedícím s
kyslíkem (např.u methanolu methylová).
Alkylová skupina (u sekundárních a
terciárních alkoholů alkylové skupiny)
vnášejí elektronovou hustotu na kyslík a
způsobují jeho částečně záporný
náboj.Při odštěpení vodíkového kationtu
(tzn. projevu kyseliny) tento částečně
záporný náboj náboj oddaluje celkový náboj
na kyslíku od nuly /-1-d/ > /-1/. Z toho
plyne, že částečně záporný náboj
zhoršuje podmínky pro odštěpování
vodíkového kationtu, takže alkohol je
zásaditější než voda a pH má větší
než 7. |
 |
| kyselina |
<-- |
------- |
--------> |
konjugovaná
zásada |
|
|
| ROH |
+ |
H2O |
 |
OH- |
+ |
H3O+ |
| alkohol |
|
zásada |
<-------- |
----------- |
--> |
konjugovaná
kyselina |
|
|
|
|
 |
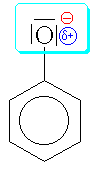 |
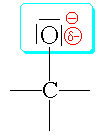
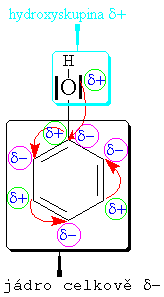
U
fenolu působí +M efekt, neboť volné
elektronové páry se snaží zapojit do
konjugace elektronů v benzenovém
jádře. To způsobuje částečný
kladný náboj na kyslíku. V případě
odštěpení vodíkového kationtu (tzn.
projevu kyseliny) tento částečně
kladný náboj přibližuje celkový
náboj na kyslíku k nule /-1+d/
</-1/. Z toho plyne, že
částečně kladný náboj podporuje
odštěpování vodíkového kationtu,
takže fenol
je kyselejší než voda (starý název - kyselina
karbolová)
a pH má
menší než 7.
| kyselina |
<-- |
------- |
--------> |
konjugovaná
zásada |
|
|
| C6H5OH |
+ |
H2O |
 |
C6H5O- |
+ |
OH- |
| fenol |
|
zásada |
<-------- |
----------- |
--> |
konjugovaná
kyselina |
|
|
| .Porovnej
s vlivem efektů na pH u aminosloučenin |
|