| Esterifikace
je reakce alkoholu s kyselinou nebo s jejím derivátem |
Esterifikace
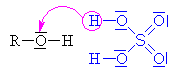
s anorganickou kyselinou
 |
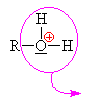 |
Součástí
esteru není kyslík z alkoholu.
Je to způsobeno mechanismem, kdy se na kyslík z
alkoholu napojuje vodík a vzniklý
alkyloxoniový kation se odpojuje. |
|
| Esterifikace
s organickou kyselinou |
 |
Součástí
esteru je kyslík z alkoholu.
Je to způsobeno mechanismem, kdy se za pomoci
katalyzáru vytvoří na uhlíku karboxyskupiny
náboj plus a na něho se poté napojí volným
elektronovým párem kyslík z alkoholu, který
se tak po odpojení vodíkového kationtu
zabuduje do molekuly esteru.. |
 |
  |
|
| Porovnání
esterifikace s organickou kyselinou v kyselém a
neutrálním prostředí (myšleno bez
použití minerální kyseliny) |
 |
 |
V kyselém prostředí
napomáhá velmi účinně kyslík z minerální
kyseliny vytvořit na uhlíku karboxyskupiny
kladný náboj.Esterifikace
je snadnější. |
 |
 |
V neutrálním
prostředí (myšleno bez
použití minerální kyseliny) se využívá
pouze částečně kladně nabitého uhlíku z
karboxyskupiny (zásluhou
elektronegativnějšího kyslíku a vazby p).Esterifikace je obtížnější. |
|









