| Schématický zápis: |
|
|
| Podrobný zápis: |
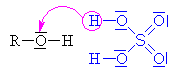
| Kyselina sírová se chová jako kyselina a alkohol
jako zásada, to
znamená, že volný elektronový pár na kyslíku v
alkoholu přijímá vodík a vzniká alkyloxoniový
kationt (kyslík má pouze 5 elektronů a proto má
náboj plus). Chybějící elektron získává
heterolytickým odštěpením od uhlíku.Odštěpovaná
voda je nahrazována mechanismem nukleofilní substituce
Sn (porovnej s halogenderiváty).
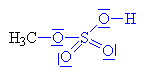
Nukleofilním činidlem je hydrogensulfát (zde je
použit mechanismus molekulární Sn1, mechanismus Sn2 ukázán dole nebo zde klikni). |
 |
 |
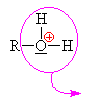
alkyloxoniumhydrogensulfát
 |
 |
|
| |
|
|
 |
| |
-H2O |
|
|
|
| Vzniklý karbokation se spojuje s
hydrogensulfátovým aniontem za vzniku anorganického
esteru alkoholu a kyseliny sírové. |
| |
|
|
 |
| |
-H2O |
|
|
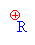 |
|
 |
 |
alkylhydrogensulfát
(kys.
alkylsírová) |
 |
|
|
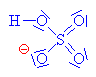
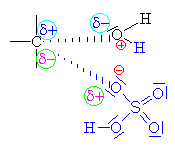
| Zde obecně
znázorněna substituce bimolekulovým
mechanismem Sn2
|
 |
|


