| Schématický zápis: |
|
|
| Podrobný
zápis (při zanedbání vlivu
katalyzátoru kyseliny sírové na mechanismus reakce): |
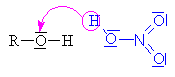
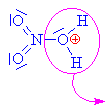
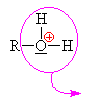
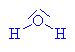
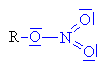
| Kyselina dusičná se chová jako kyselina a alkohol
jako zásada, to
znamená že volný elektronový pár na kyslíku v
alkoholu přijímá vodík a vzniká alkyloxoniový
kationt (kyslík má pouze 5 elektronů a proto má
náboj plus). Chybějící elektron získává
heterolytickým odštěpením od uhlíku. |
|
|
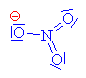
| Vzniklý karbokation se spojuje s nitrátovým
aniontem za vzniku anorganického esteru alkoholu a
kyseliny dusičné. |
| |
|
|
 |
| |
-H2O |
|
|
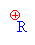 |
 |
 |
 |
| alkylnitrát (kys.
alkyldusičná) |
 |
|
|
| Podrobný
zápis (uvažující i
vliv kyseliny sírové na mechamismus reakce): |
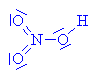
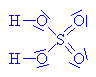
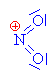
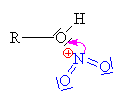
| Kyselina sírová a kyselina
dusičná vytváří
tzv. nitrační směs. Kyselina sírová
daruje vodíkový kation (Lewisova kyselina) kyselině dusičné
(Lewisova kyselina)-
váže se na volný elektronový pár u kyslíku v
hydroxyskupině |
|
|
|
|
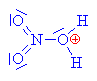
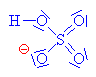
| Kation odštěpuje vodu a vzniká
tak nitroniový kation, který je elektrofilním
činidlem |
|
|
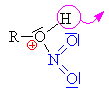
| Nitroniový kation napadá volný elektronový pár u
kyslíku v hydroxyskupině alkoholu. U vzniklého
karbokationtu se poté odštěpuje vodíkový kation. |
 |
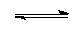 |
alkylnitrooxonium
 |
|
| |
|
|
 |
| |
-H+ |
|
|
alkylnitrát (kys.alkyldusičná)
 |
|
|
|
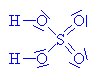
| Odštěpený vodíkový kation se napojuje na hydrogensulfátový anion
a za vzniku kyseliny
sírové (ta tedy slouží jako katalyzátor) a ta rozbíhá další kolo reakce |
|
|